Ústav chemie
VÝZNAMNÉ VÝSLEDKY VĚDECKO-VÝZKUMNÉ ČINNOSTI
ÚSTAV CHEMIE (2015–2025)
Tým z Ústavu chemie získal prestižní Cenu Wernera von Siemense za nejlepší diplomovou práci
Cenu Wernera von Siemense za první místo v kategorii Nejlepší diplomová práce získal Ing. Jiří Navrátil z Fakulty technologické Univerzity Tomáše Bati ve Zlíně za diplomovou práci s názvem Syntéza ligandu na bázi 4,9-disubstituovaného diamantanu a studium jeho supramolekulárních vlastností.



Práce Jiřího Navrátila se zabývá studiem tvorby supramolekulárních komplexů typu hostitel–host, kde v roli hostitelských molekul vystupují makrocyklické sloučeniny z rodiny cyklodextrinů a cucurbit[n]urilů, a v roli hostující molekuly ligand na bázi axiálně disubstituovaného diamantanu. Cílem práce bylo připravit příslušný ligand a následně detailně prozkoumat jeho supramolekulární chování. Získané výsledky byly překvapivé a velmi zajímavé: jedná se o první dikationtový ligand na bázi diamantanu tvořící velmi stabilní hostitel–host komplexy s makrocykly z rodiny cyklodextrinů a současně o první práci popisující schopnost diamantanové klece tvořit v danou chvíli supramolekulární komplexy s více než jednou (stejnou nebo různou) makrocyklickou sloučeninou.
Sloučenina, která na sebe nechala tři roky čekat
Diamantanoidy nemají ve svém názvu obsaženo slovo „diamant“ jen tak náhodou. Obecně lze jejich struktury odvodit od základních stavebních jednotek diamantu – známého nerostu složeného pouze z atomů uhlíku. Nejmenším z řady diamantanoidů je adamantan, tricyklický uhlovodík izolovaný ve 30. letech 20. století Stanislavem Landou z hodonínské ropy. „Chemií adamantanu se v naší výzkumné skupině zabýváme již více než 20 let,“ říká vedoucí práce Michal Rouchal a dodává: „Druhým v řadě je diamantan, který se od adamantanu neliší jen svojí velikostí, ale také možností axiální disubstituce (oba substituenty v jedné přímce), což se z pohledu návrhu nových vazebných motivů pro supramolekulární hostitel–host systémy jevilo jako velmi zajímavé a výhodné. Proto jsme se rozhodli vypsat na toto téma diplomovou práci.“
„Představa, že mým úkolem bude syntetizovat molekulu s doposud nepopsanou strukturou, a pakliže budu úspěšný, budu se moci věnovat studiu jejího supramolekulární chování, mě ihned zaujala. Právě skutečnost, že budu první, kdo tuto látku připraví, mne na tom asi fascinovala nejvíce. Proto jsem se s chutí, hned v létě mezi prvním a druhým ročníkem, vrhl do práce, čímž započala moje téměř tříletá cesta směrem ke kýženému ligandu,“ vzpomíná Jiří Navrátil.
Cesta k cíli nebyla jednoduchá. První desítky miligramů vysněného ligandu držel Jiří v rukou až po třech letech „syntetické dřiny“, kdy v některých případech bylo zapotřebí pečlivě optimalizovat reakční podmínky. Trpělivost a vynaložené úsilí se nakonec vyplatily. Nový diamantanový ligand všechny překvapil svými neočekávanými vlastnostmi. „Jirkovy výsledky jsou nejen velmi zajímavé, ale především cenné. Zejména schopnost ligandu vázat více makrocyklů těsně u sebe umístěných na jedno vazebné místo, a pravděpodobně v různých vzájemných orientacích, přináší do světa hostitel–host chemie mnoho nového a otevírá dveře doposud zavřené nebo pouze pootevřené,“ dodává Michal Rouchal.
Poslat přihlášku bylo dobré rozhodnutí
Dobré téma, velmi zajímavé výsledky, nadprůměrně kvalitní rukopis. To si podle Michala Rouchala o přihlášení do soutěže o cenu Wernera von Siemense přímo říkalo. Pro Jiřího bylo motivací zjistit, jak si jeho diplomová práce povede v obrovské konkurenci, která v soutěži každoročně panuje. Že z toho nakonec bude první místo, ale ani jednoho z nich nenapadlo.


Získaného ocenění si Jiří i Michal velmi cenní, zároveň ale dodávají, že se jedná o úspěch celého týmu supramolekulární chemie pod vedením Roberta Víchy, v širším kontextu pak Fakulty technologické a Univerzity Tomáše Bati ve Zlíně.
Zde se můžete podívat na YouTube medailonek: Syntéza ligandu na bázi 4,9-disubstituovaného diamantanu a studium jeho supramolekulárních vlastností
V. Kolařík, A. Hromádková, A. Knirsch, Z. Prucková, P. Janovský, M. Rouchal, J. S. Ward, K. Rissanen, R. Vícha: Metal cations switch geometry of b-cyclodextrin complexes.
Chemical Communications 2025, 61, 7077–7080. (IF2024 = 4,2) | online
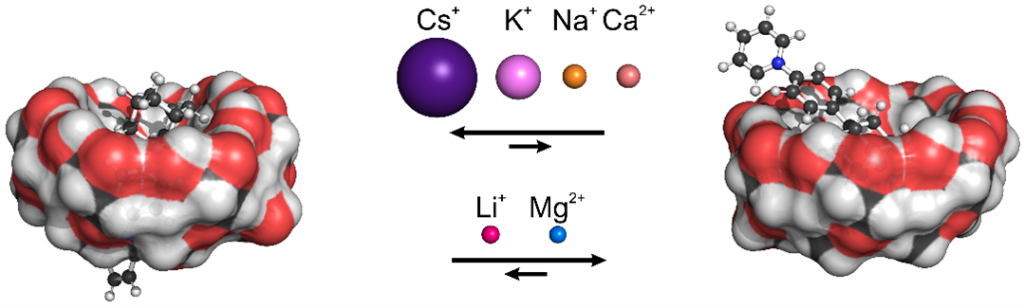
Udělali jsme další krok v poznání řízení supramolekulárních komplexů. Povedlo se nám totiž připravit komplexy cyklodextrinů, jejichž preferovanou geometrii v roztoku jsme schopni měnit.
Jak přesně toho můžeme dosáhnout? Stačí přidat jeden ekvivalent β-cyklodextrinu, jeden ekvivalent ligandu, a nakonec to pořádně osolit chloridy různých kationtů. Zjistili jsme totiž, že různé kovové ionty, v závislosti na jejich van der Waalsově poloměru, podporují vznik jedné ze dvou možných geometrických forem. Objemnější ionty preferují širší sekundární okraj β-cyklodextrinu, čímž vytlačují kationtovou část ligandu směrem k užšímu primárnímu okraji, a naopak.
A. Závodná, P. Janovský, V. Kolařík, J. S. Ward, Z. Prucková, M. Rouchal, K. Rissanen, R. Vícha: Allosteric release of cucurbi[6]uril from a rotaxane using a molecular signal.
Chemical Science 2025, 16, 83–89. (IF2024 = 7,4) | online | Inside back cover | Napsali o nás
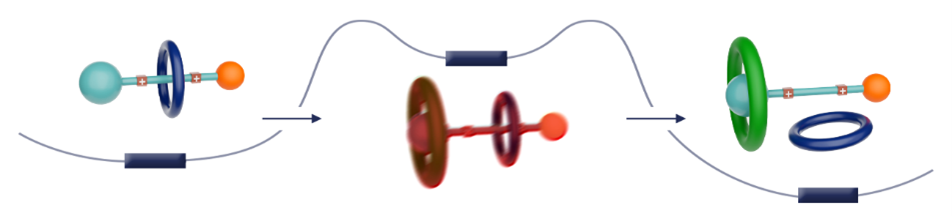
Rotaxany, často přirovnávané k náhrdelníku obepínajícímu krk bez jakékoliv přímé spojky, jsou známé pro své mechanicky uzamčené struktury. Problémem však vždy bylo, jak jednotlivé komponenty oddělit bez jejich poškození. Klíčovým řešením tohoto projektu se stalo využití odpudivých interakcí mezi dvěma homology makrocyklických sloučenin z rodiny cucurbiturilů. Tyto interakce se ukázaly být natolik silné, že umožnily překonat energetickou bariéru mechanické vazby. Vazba signálního makrocyklu na adamantanové regulační místo pak sehrála rozhodující roli v celém procesu. Naším dalším cílem bude inkorporovat objevený spínač do větších molekul nebo jej využít pro řízení rovnovážných koncentrací v multikomponentních systémech.
P. Janovský, A. Springer, J. Filip, Z. Prucková, M. Nečas, M. Rouchal, C. A. Schalley, R. Vícha: para-Phenylenediamine Dimer as a Redox–Active Guest for Supramolecular Systems.
Chemistry – A European Journal 2024, 30, e202400535. (IF2023 = 3,9) | online
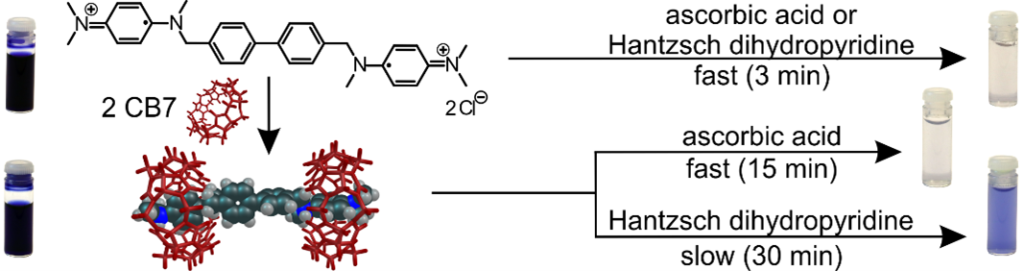
Redoxní motivy představují klíčový prvek nejen v supramolekulárních molekulových strojích a přepínačích. Jedním z takových motivů je p-fenylendiamin, který byl dosud v supramolekulárních systémech spíše opomíjen. V této práci jsme jej využili ke konstrukci tritopického ligandu s cílem detailně prostudovat jeho supramolekulární chování vůči makrocyklům z rodiny cucurbit[n]urilů a cyklodextrinů. Ukázalo se, že tento motiv představuje vhodné vazebné místo pro zkoumané makrocykly jak v základním, tak i v oxidovaném stavu. Komplexace přitom významně ovlivňuje jak dimerizaci motivů, tak jejich redoxní chování, a v závislosti na typu makrocyklu vede například ke stabilizaci reaktivních kation-radikálů ve vodném prostředí. Tato zjištění představují důležitý krok pro návrh redoxně řízených supramolekulárních strojů.
M. Jurtík, B. Gřešková, Z. Prucková, M. Rouchal, L. Dastychová, L. Vítková, K. Valášková, E. Achbergerová, R. Vícha: Assembling a supramolecular 3D network with tuneable mechanical properties using adamantylated cross-linking agents and b-cyclodextrin-modified hyaluronan.
Carbohydrate Polymers 2023, 313, 120872. (IF2022 = 11,2) | online
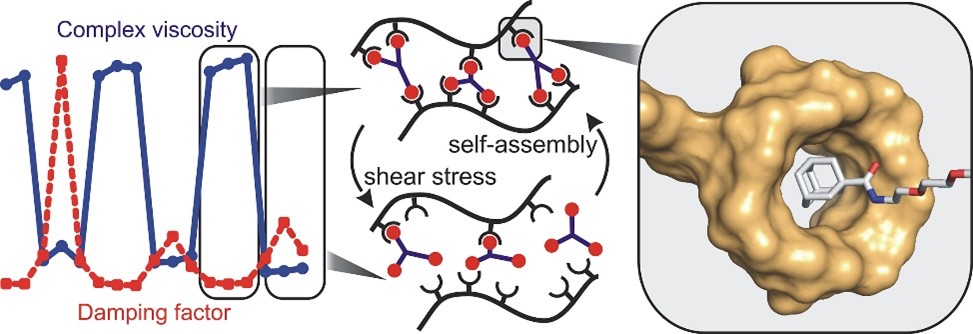
Hydrogely založené na interakcích typu hostitel–host jsou obvykle připravovány tak, že se provede chemická modifikace dvou polymerních řetězců, kdy na jeden jsou zavedeny makrocyklické sloučeniny (hostitel) a na druhý vhodný ligand (host). Tento způsob s sebou přináší určité komplikace, proto jsme se rozhodli k cyklodextrinem modifikované kyselině hyaluronové přidat ligandy na bázi adamantanu, které fungovaly jako spojky mezi jednotlivými polymerními řetězci. Ukázalo se, že použití různých typů spojek ovlivňuje pevnost a pružnost výsledného hydrogelu. Připravené hydrogely navíc disponují zajímavými vlastnostmi, jako například schopností reverzibilní samo skladby. Tento přístup otevírá novou cestu k přípravě responzivních hydrogelů, které by mohly nalézt uplatnění v materiálovém inženýrství nebo medicínských aplikacích.
K. Jelínková, A. Závodná, J. Kaleta, P. Janovský, F. Zatloukal, M. Nečas, Z. Prucková, L. Dastychová, M.Rouchal, R. Vícha: Two Squares in a Barrel: An Axially Disubstituted Conformationally Rigid Aliphatic Binding Motif for Cucurbit[6]uril.
The Journal of Organic Chemistry 2023, 88, 15615–15625. (IF2022 = 3,6) | online
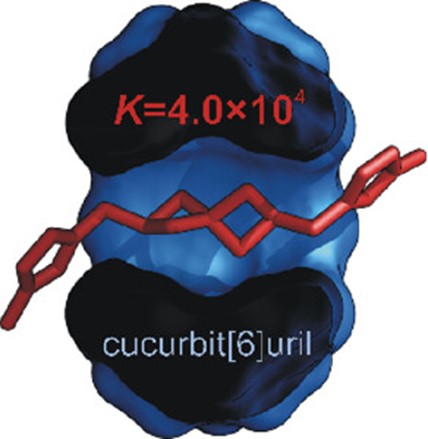
Rodina cucurbiturilových makrocyklů zahrnuje několik homologů lišících se počtem glykolurilových jednotek a s tím související velikostí kavity. Zatímco pro objemnější homolog, cucurbit[7]uril, je známa celá řada vazebných motivů na bázi klecových uhlovodíků s velmi vysokými asociačními konstantami, pro menší, cucurbit[6]uril (CB6), byly dosud popsány jen motivy odvozené od flexibilních alifatických uhlovodíků. V naší práci popisujeme přípravu dvou nových vazebných motivů odvozených od spiro[3.3]heptanu a bicyklo[1.1.1]pentanu a jejich schopnosti vázat se do dutiny CB6. Přestože asociační konstanta komplexu CB6 a spiroheptanového ligandu dosahuje pouze hodnoty 4×104, je velmi cenná možnost využít tohoto rigidního systému pro konstrukci složitějších vícevazebných ligandů.
J. Tomeček, A. Čablová, A. Hromádková, J. Novotný, R. Marek, I. Durník, P. Kulhánek, Z. Prucková, M. Rouchal, L. Dastychová, R. Vícha: Modes of micromolar host–guest binding of b-cyclodextrin complexes revealed by NMR spectroscopy in salt water.
The Journal of Organic Chemistry 2021, 86, 4483–4496. (IF2020 = 4,4) | online
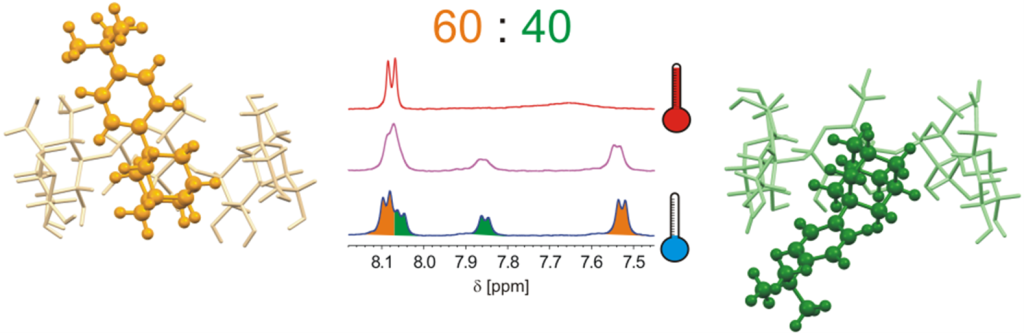
Určování struktury supramolekulárních útvarů, které vykazují v daném prostředí, a za daných podmínek, rychlou dynamiku není snadné, protože pozorované spektrální charakteristiky odpovídají průměru hodnot všech přítomných geometrických uspořádání. Obvykle tak ani není zřejmé, kolik takových uspořádání je v rovnovážné směsi přítomno. Nám se podařilo vypracovat metodiku spočívající v měření NMR spekter v koncentrovaném slaném roztoku při teplotách pod 0 °C a takto poprvé pozorovat a plně strukturně charakterizovat (pomocí 2D NMR experimentů) komplexy nově připravených adamantylfenylových ligandů. Tyto poznatky jsou velmi důležité pro smysluplné navrhovaní složitějších supramolekulárních funkčních systémů, například molekulárních regulovatelných katalyzátorů, na jejichž přípravě dlouhodobě pracujeme.
S. Kulkarni, K. Jelínková, M. Nečas, Z. Prucková, M. Rouchal, L. Dastychová, P. Kulhánek, R. Vícha: A photochemical/thermal switch based 4,4´-bis(benzimidazolio)stilbene: Synthesis and supramolecular properties.
ChemPhysChem 2020, 21, 2084–2095. (IF2019 = 3,1) | online
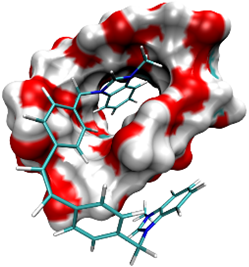
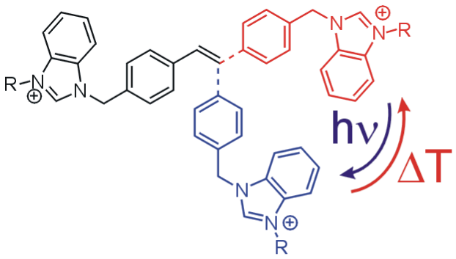
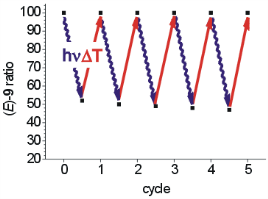
Deriváty stilbenu patří k dlouhodobě studovaným strukturám vzhledem k jejich schopnosti podléhat fotochemicky či termálně indukované isomerizaci na dvojné vazbě. Takové systémy mohou fungovat jako molekulární spínače reagující na světelné nebo tepelné podněty. My jsme připravili a popsali strukturu bis-imidazoliových derivátů stilbenu (b), které jsou v podobě komplexů s cyklodextriny (a) snadno rozpustné ve vodném prostředí. Ukázalo se, že komplexace s b-cyklodextrinem nemá vliv na isomerizační reakce. Pomocí UV záření bylo možné tyto látky převést na termodynamicky méně stabilní cis-formu, která při zahřátí roztoku opět přecházela na stabilnější trans-formu. Tyto cykly bylo možné několikrát opakovat (c). Do článku se již nevešla informace, že k fotochemické isomerizaci není nutné používat silný zdroj UV záření (v našem případě středně-tlaková Hg výbojka s výkonem 125 W), ale izomerizaci lze stejně efektivně realizovat jen za pomoci denního světla, jak jsme zjistili jednoho slunečného dne na střeše Laboratorního centra Fakulty technologické.
Cubane Arrives on the Cucurbituril Scene (2017)
Jelínková, H. Surmová, A. Matelová, M. Rouchal, Z. Prucková, L. Dastychová, M. Nečas, R. Vícha: Cubane Arrives on the Cucurbituril Scene.
Organic Letters 2017, 19, 2698–2701. (IF2016 = 6,579)
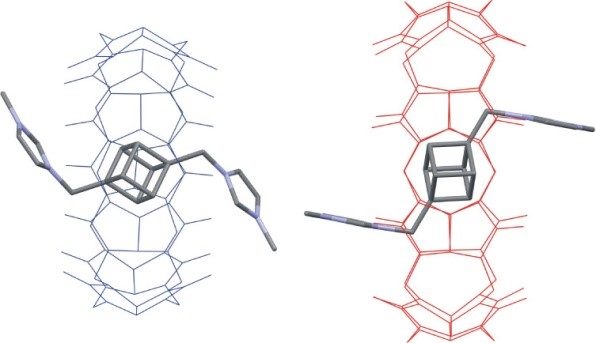
Klecové uhlovodíky představují velmi zajímavé základní struktury pro přípravu supramolekulárních ligandů s velmi vysokými afinitami k některým makrocyklům, například cucurbiturilům (CBn). Deriváty velmi zajímavého uhlovodíku kubanu stály až dosud stranou zájmu chemiků. V této publikaci popisujeme přípravu prvního známého dikationtového kubanového ligandu a jeho supramolekulární chování ve směsích s cyklodextriny a cucurbiturily. K velmi zajímavým výsledkům patří úspěšná příprava monokrystalu komplexu tohoto ligandu s CB7 a CB7 a popis struktury pomocí RTG difrakční analýzy.
Cooperative binding of cucurbit[n]urils and b-cyclodextrin to heteroditopic imidazolium-based guests (2016)
Branná, J. Černochová, M. Rouchal, P. Kulhánek, M. Babinský, R. Marek, M. Nečas, I. Kuřitka, R. Vícha:
Cooperative binding of cucurbit[n]urils and b-cyclodextrin to heteroditopic imidazolium-based guests.
Journal of Organic Chemistry 2016, 81, 9595–9604. (IF2016 = 4,849)
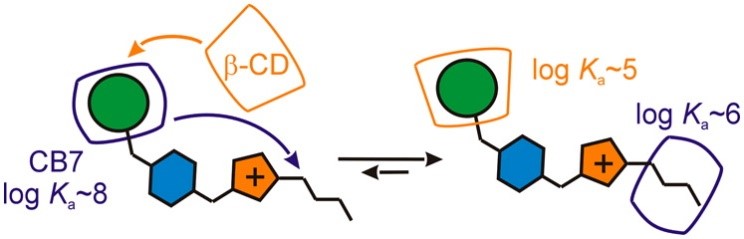
Vícevazebné ligandy pro supramolekulární systémy se ukazují jako slibné komponenty například pro konstrukci molekulárních senzorů či přepínačů. S rostoucí složitostí těchto ligandů ale zároveň roste počet možností konečného uspořádání supramolekulárních útvarů. Navíc se ukazuje, že na výslednou podobu komplexů mají zásadní vliv i jevy, které se nemohly projevit při studiu jednovazebných modelů. Mezi tyto jevy patří například vzájemné interakce mezi vázanými makrocykly nebo soutěžení vazebných míst v rámci jednoho komplexu. Důsledkem těchto sekundárních jevů může být zcela jiné uspořádání výsledného komplexu než by napovídaly individuální preference vazebných míst. V této publikaci jsme popsali přípravu několika ligandů se dvěma vazebnými místy, popsali kvantitativně interakce mezi makrocykly a připravili jeden supramolekulární systém s geometrií odporující původním očekáváním.
Rotaxanes capped with hosts: supramolecular behavior of adamantylated bisimidazolium salts containing a biphenyl centerpiece (2015)
Branná, M. Rouchal, Z. Prucková, L. Dastychová, R. Lenobel, T. Pospíšil, K. Maláč, R. Vícha:
Rotaxanes capped with hosts: supramolecular behavior of adamantylated bisimidazolium salts containing a biphenyl centerpiece.
Chemistry – A European Journal 2015, 21, 11712–11718. (IF2016 = 5,317)
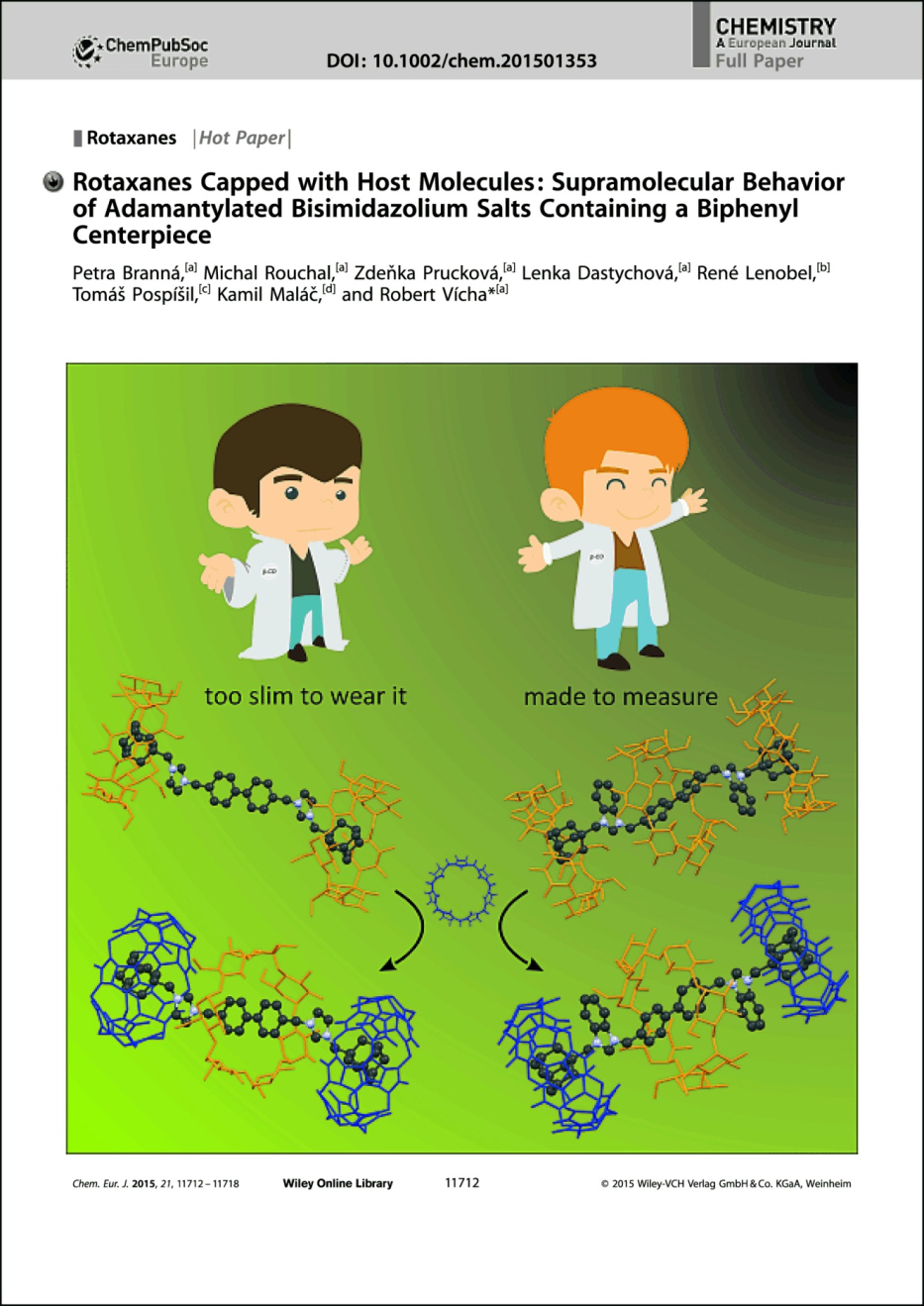
V této publikaci popisujeme přípravu a supramolekulární chování ligandů se třemi vazebnými místy. Nejzajímavější zjištění bylo, že více stericky bráněný ligand pevněji vázal některé makrocykly a umožnoval tak navázání více jednotek makrocyklu než ligand, který mohl makrocykly volně prokluzovat. Dále jsme v této práci demonstrovali možnost připravit rotaxanové struktury, tedy uspořádání molekul s jedním makrocyklem uvězněným na ose ligandu pomocí dvou supramolekulárních uzávěrů. Výhoda proti kovalentním uzávěrům spočívá v možnosti vyvolání rozpadu tohoto rotaxanu přidáním kompetitoru pro makrocykly sloužící jako uzávěry. Toto zjištění má velký význam při návrhu a konstrukci molekulárních strojků.
Design, Synthesis and Antitubercular Potency of 4-Hydroxyquinolin-2(1H)-ones (2017)
Macedo de, M. B.; Kimmel, R.; Urankar, D.; Gazvoda, M.; Peixoto, A.; Cools, F.; Torfs, E.; Verschaeve, L.; Lima, E. S.; Lyčka, A.; Milićević, D.; Klásek, A.; Cos, P.; Kafka, S.; Košmrlj, J.; Cappoen, D.:
Design, Synthesis and Antitubercular Potency of 4-Hydroxyquinolin-2(1H)-ones.
Euopean Journal of Medicinal Chemistry 2017, 138, 491-500. (IF2016 = 4,519)
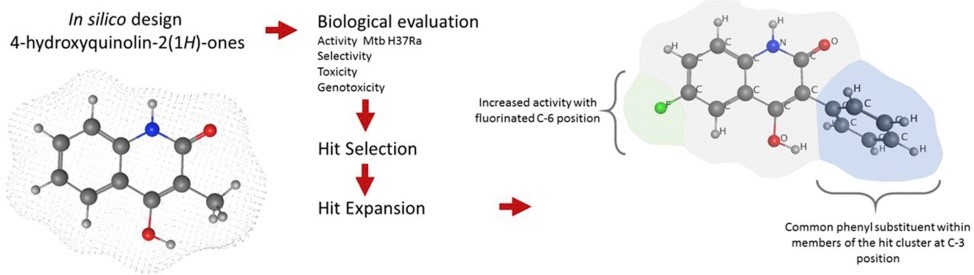
V této studii, otištěné v jednom z nejprestižnějších časopisů z oblasti medicinální chemie, byly navrženy 50-členná knihovna substituovaných 4-hydroxychinolin-2(1H)-onů a dva úzce příbuzné analogy. Všechny sloučeniny byly ohodnoceny in-silico z hlediska podobnosti s léčivy a následně syntetizovány. Třináct derivátů s fenylovou skupinou v poloze 3 vykazovalo minimální inhibiční koncentraci vůči Mycobacterium tuberculosis H37Ra nižší než 10 mM a vůči Mycobacterium bovis AN5A nižší než 15 mM, avšak tyto sloučeniny byly neaktivní vůči rychle rostoucím druhům mykobakterií. Žádný z vybraných derivátů nevykazoval akutní toxicitu vůči buňkám MRC-5 ani časné známky genotoxicity v testu Vitotox™ v rozmezí aktivních koncentrací. Studie vztahu struktura-aktivita poskytla určitou představu o další příznivé substituci skeletu 4-hydroxychinolin-2(1H)-onu a nakonec jako nejslibnější člen knihovny byl vybrán 6-fluor-4-hydroxy-3-fenylchinolin-2(1H)-on s hodnotou MIC 3,2 mM a s hodnotou CC50 vůči MRC-5 67,4 mM.
Synthesis of 1,4-Benzodiazepine-2,5-diones by Base Promoted Ring Expansion of 3-Aminoquinoline-2,4-diones (2017)
Křemen, F.; Gazvoda, M.; Kafka, S.; Proisl, K.; Srholcová, A.; Klásek, A.; Urankar, D.; Košmrlj, J.:
Synthesis of 1,4-Benzodiazepine-2,5-diones by Base Promoted Ring Expansion of 3-Aminoquinoline-2,4-diones.
Journal of Organic Chemistry 2017, 82, 715-722. (IF2016 = 4,849)

V článku je popsána reaktivita 3-aminochinolin-2,4-dionů, která dosud neměla obdobu. Tyto sloučeniny v zásaditém prostředí podléhají molekulárnímu přesmyku, jehož produkty jsou 1,4-benzodiazepin-2,5-diony. Přeměna probíhá za mírných podmínek při použití 1,1,3,3-tetramethylguanidinu, ethoxidu sodného nebo benzyltrimethylamonium-hydroxidu jako báze. Navržený mechanismus přesmyku a konformační rovnováha 1,4-benzodiazepin-2,5-dionových kruhů jsou předmětem diskuse.
Indolization of N-(α-Ketoacyl)anthranilic Acids into 2-(Indol-2-carboxamido)benzoic Acids and 2-Indolyl-3,1-benzoxazin-4-ones and Their NMR Study (2014)
Proisl, K.; Kafka, S.; Urankar, D.; Gazvoda, M.; Kimmel, R.; Košmrlj, J.:
Fischer Indolization of N-(α-Ketoacyl)anthranilic Acids into 2-(Indol-2-carboxamido)benzoic Acids and 2-Indolyl-3,1-benzoxazin-4-ones and Their NMR Study.
Organic & Biomolecular Chemistry 2014, 12, 9650-9664.
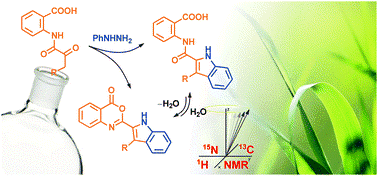
Reakcí N-(α-ketoacyl)anthranilových kyselin s fenylhydraziniumchloridem ve vroucí kyselině octové byly připraveny 2-(indol-2-karboxamido)benzoové kyseliny s dobrými až vynikajícími výtěžky a 2-indolyl-3,1-benzoxazin-4-ony jako vedlejší produkty. Tvorba uvedených vedlejších produktů může být snadno potlačena hydrolytickým zpracováním. Alternativně zvýšením reakční teploty nebo prodloužením reakční doby mohou být získány výhradně 2-indolyl-l-benzoxazin-4-ony. Studie byla zaměřena na optimalizaci reakčních podmínek, rozsah výchozích sloučenin a průběh jejich přeměn. Produkty byly characterizovány 1H-, 13C- a 15N-NMR spektry. Rezonance byly přiřazeny na základě standardních 1D a vybraných 2D NMR experimentů (1H–1H gs-COSY, 1H–13C gs-HSQC, 1H–13C gs-HMBC) s 1H–15N gs-HMBC jako praktickým nástrojem pro stanovení chemických posunů v 15N-NMR spektrech při přirozeném zastoupení isotopu 15N.